
Mesure de la taille d'une molťcule d'huile
But : parvenir ŗ connaÓtre la taille d'une molťcule d'huile.
He bien oui : il est possible d'avoir une mesure concrŤte de la taille d'une molťcule d'huile, de maniŤre assez aisťe, mÍme si elle requiert un peu de patience et de doigtť.
L'expťrience :
Se munir d'un rťcipient de grande surface (par exemple, une soucoupe propre de pot de fleur ou un ťvier remplis d'eau). Remplissez ce rťcipient de quelques centimŤtres d'eau. Soupoudrez du talc fin ŗ la surface de l'eau, en une trŤs fine couche ŗ peu prŤs partout (n'en mettez pas trop !). Prenez ŗ prťsent un fil rigide, genre fil de fer. C'est lŗ que les choses sťrieuses commencent : trempez ce fil dans l'huile et faites tomber une goutte d'huile (seulement une goutte) au centre de votre surface de talc. Attention, il faut ťviter ŗ la fois de faire toucher le fil avec la surface de l'eau et de faire tomber la goutte de trop haut. Lorsque la goutte est dans l'eau, on observe que le talc est repoussť vers les bords par l'ťtallement de cette goutte. Il ne reste plus qu'ŗ mesurer le diamŤtre de la zone sans talc, et de passer ŗ la partie calculs !
Conseils :
La chute de la goutte pose parfois quelques problŤmes. Voilŗ comment les rťsoudre :
- Un fil plus long permet ŗ la goutte d'Ítre plus grosse en arrivant ŗ la base du fil. Elle tombera alors plus facilement.
- En rťchauffant lťgŤrement l'huile, elle sera plus liquide est la goutte roulera plus facilement le long du fil.
- Toutes les huiles ne se valent pas forcťment : c'est ŗ vous de tester et de me faire part de vos tentative dont j'informerai les futurs visiteurs.
- Des personnes ont tentť de remplacer le talc par de la farine. Visiblement, cela ne fonctionne pas.
Les calculs :
Pas d'inquiťtude illťgitimes, se sont des calculs extrťmements basiques (je suis sŻr qu'ils sont faisables ŗ partir du CM voire avant).
1) Calcul du volume de la goutte.
Calculons le volume de la goutte que vous avez fait tomber. Nous allons dire qu'elle ťtait ŗ peu prŤs ronde et qu'elle faisait disons 1 millimŤtre de diamŤtre (ce ne sera pas trŤs prťcis, mais c'est un ordre de grandeur que l'on souhaite). Volume d'une sphŤre : V1=4*Pi*r*r*r/3 oý r est le rayon de la goutte et Pi=3,141592Ö Notre goutte a donc un volume de 4.19mm3 environ.
2) Calcul de la taille de la molťcule.
On considŤrera que la tache obtenue sur l'eau est circulaire. En rťalitť, mais on ne le voit pas, c'est un cylindre de hauteur la taille d'une molťcule. Volume d'un cylindre : V2=Pi*R*R*h oý R est le rayon de la tache, h la hauteur d'une molťcule. Comme l'huile n'a pas disparu depuis que la goutte est tombťe, on a V1=V2.
Donc h=(4*r*r*r)/(3*R*R) avec les mÍmes notations que prťcťdemment. Et voilŗ, on a la taille de notre molťcule d'huile !
Analyse physique : Une molťcule d'huile est en fait en 2 parties : elle est constituťe d'une " tÍte " hydrophile (qui aime l'eau) et d'une " queue " hydrophobe (qui n'aime pas l'eau). A la surface de l'eau, votre goutte d'huile va donc s'ťtaler pour que toutes les tÍtes se retrouvent en contact avec l'eau et que toutes les queues se retrouvent pointťes vers le haut. La tache a donc l'ťpaisseur d'une molťcule. Cette double nature de la molťcule d'huile est trŤs important : elle est pas exemple la cause des bulles observťes dans la premiŤre expťrience. Notons que les produits vaisselle ont ŗ cúur de rendre les queues de ces molťcules hydrophiles pour pouvoir les ťliminer avec l'eau.
Molťcule d'huile : queue
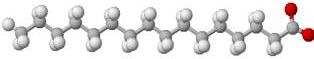 tÍte.
tÍte.En gris : atomes de carbone. En blanc : atomes d'hydrogŤne. En rouge : atomes d'oxygŤne.
Historique : Cette expťrience a, ŗ l'origine, ťtť rťaliťe par Benjamin Franklin qui a versť de l'huile sur un lac et mesurť ainsi la taille d'une molťcule (je ne me souviens plus de l'annťe Ö). Aujourd'hui, cette expťrience est courrement rťalisťe en Travaux Pratiques au lycťe, en seconde.
| Prťcťdent | Menu expťrience | Suivant |